Descrição da exploração
Trata-se de uma exploração de baterias (sítio 2) que faz parte de uma exploração que funciona em bandas onde se desmamam 85-90 ninhadas de três em três semanas (900-1.000 leitões/desmame). Os leitões chegam com uma idade média de 26 - 28 dias e com um peso médio de 7,4 - 7,6 kg.


Foto 1. Exterior do pavilhão.
Estas baterias funcionam em fluxo contínuo – entra um novo lote a cada três semanas – tendo pelo menos dois grupos de leitões sempre presentes. A estrutura consiste basicamente em três salas adjacentes onde se realiza tudo dentro/tudo fora (TD/TF). Os parques, de uns 29 leitões cada, dispõem de solo de slat de betão/plástico, alimentação ad libitum em comedouros lineares e um número adequado de bebedouros tipo chucha. A ventilação é semi-natural com extractores e com aquecimento por ar quente. A higiene e o maneio podem classificar-se como de nível médio-alto.

Foto 2. Interior das baterias.
O estatuto sanitário é elevado (negativo a PRRS, Aujeszky, App, rinite atrófica). Os leitões foram vacinados contra a M. hyo na maternidade e, ao chegarem às baterias, não costumam reciber nenhum tratamento. No passado houve alguns problemas esporádicos de meningite ou morte súbita por Streptococcus suis que foram resolvidos medicando com amoxicilina na água de bebida (algumas vezes na ração).
Até Novembro de 2011 os resultados técnicos destas baterias foram discretos em baixas (mortos e sacrificados) inferiores a 4%, crescimento diário superior a 450 g e um índice de conversão de 1,6 - 1,7.
Aparecimento da sintomatologia, testes laboratoriais e diagnóstico
.
De repente, a finais de Novembro de 2011, o proprietário detecta um aumento da mortalidade com a perda dos "leitões mais bonitos" do grupo mais velho (grupo A), que tinha entrado a 20 de Outubro. Os leitões estavam há 30-40 dias nas baterias e, segundo o tratador, não se notava nenhuma sintomatologa em particular mas cada dia que passava encontravam-se mais animais mortos.
Na primeira visita os animais estavam activos, com bom aspecto e alimentavam-se regularmente. Não eram evidentes quaisquer problemas respiratórios ou entéricos. A necropsia, levada a cabo na própria exploração, de dois animais encontrados mortos não permitiu chegar a nenhuma conclusão devido à ausência de lesões patognomónicas ou indicativas. Recolheram-se amostras destes dois animais (zaragatoas de meninges e intestinos, baço e pulmão) que se enviaram para o laboratório onde se descartou a presença de Streptococcus ou outras bactérias que pudessem causar “morte súbita” como por exemplo E.coli hemolitico K88 (F4). Mediante PCR e exames serológicos efectuados numa amostra significativa de indivíduos dos dois grupos presentes confirmou-se que a exploração continuava a ser negativa a PRRS e Aujeszky. Como precaução prescreveu-se um tratamento com amoxicilina (20 mg/kg p.v.) na água de bebida que não deu nenhum tipo de resultado. Nos dias e semanas posteriores as perdas diárias, além de acontecerem por grupo (o segundo grupo, B, tinha entrado a 10 Novembro), também se registaram por parques, evidenciando que em alguns parques... a mortalidade tinha chegado aos 50%!
Uns dias depois, durante a necropsia de outros indivíduos, detectaram-se lesões (necrose) no miocárdio que podiam ser indicativas de Encefalomiocardovirus (EMCV).
Por este motivo enviaram-se outras amostras (leitões mortos e/ou órgãoos) para a sede de Brescia do Instituto Zooprofilático da Lombardia e da Emilia Romana (IZSLER) que confirmaram a presença de EMCV mediante PCR e cultivo celular. O departamento de Patologia da Faculdade de Veterinária da Universidade de Parma realizou exames histológicos dos cérebros e corações de outros três leitões mortos. Nos dias imediatamente posteriores recolheram-se amostras de fezes e urina de leitões de vários parques de ambos grupos para verificar se os animais podiam ser excretores de vírus.
|
 |
|
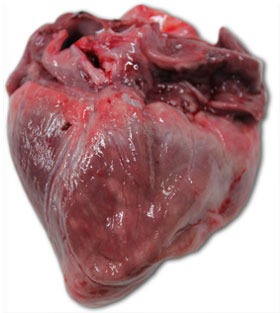
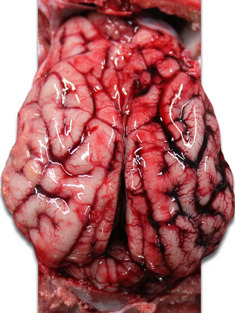
| Foto 3. Coração de leitão morto aos 40 dias de vida. Nota-se uma grande dilatação do ventrículo direito, com necrose multifocal do miocárdio (manchas brancas) e atrofia gelatinosa do tecido adiposo do epicárdio. | Foto 4. Cérebro de leitão com congestão dos vasos venosos do hemisfério cerebral direito. |
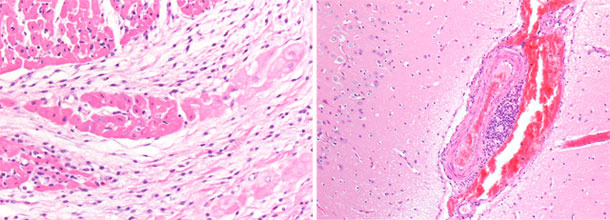
|
Foto 5. Cérebro de leitão. Engrossamento e congestão dos vasos venosos do hemisfério cerebral direito. |
Foto 6. Miocárdio, ventrículo direito. Necrose focal basófila do miocárdio com microvacuolação. |
Resumo dos resultados
Apesar de todos os esforços para controlar a propagação da infecção, as baixas – especialmente a morte súbita dos melhores leitões – do grupo A continuaram até atingir os 25%. Este grupo, quando se transferiu para a engorda, ainda perdeu mais 7% dos animais nas duas primeiras semanas de engorda. As perdas do grupo B estavam a chegar a níveis similares (18%) quando, a 1 de Dezembro, chegou à exploração o grupo C. A sequência temporal dos grupos ao desmame e as suas perdas apresentam-se no seguinte gráfico.
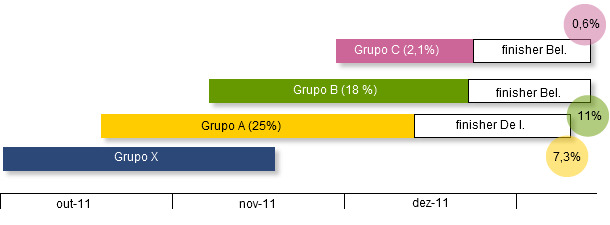
O laboratorio de patologia da Faculdade de Veterinária de Parma confirmou a presença difusa de petéquias associadas a focos de descoloração no miocárdio, indicativa de uma forma grave de miocardite e uma congestão difusa das meninges.
As dez amostras de fezes e as três de urina dos grupos A e B que foram enviadas ao IZSLER de Brescia foram todas positivas para EMCV.
Discussão
Os exames virológicos e histopatológicos confirmaram que este grave caso de mortes súbitas, registadas especialmente nos grupos A e B, eram devidos à infecção por Encefalomiocardiovirus. Segundo a literatura, os ratos e as ratazanas são portadores e difusores da infecção. Pese a que não existam dados neste sentido, é provável que uma única família de ratos/ratazanas possa desencadear inicialmente o problema. Na exploração em questão, de facto, a desratização era muito cuidadosa e não havia evidências de uma presença massiva de roedores. Não se observou presença de excrementos e só depois de uma exaustiva procura foram encontrados alguns rastos de ratos pequenos. Portanto deve haver um período – seguramente breve – durante o qual os porcos actuam como difusores/multiplicadores da infecção. Este período de tempo é provavelmente de 1 - 3 dias, o período que decorre entre o T0 – momento da infecção – e a morte do animal. Esta hipótese confirmou-se pela detecção de EMCV nas fezes e urina e a concentração da mortalidade em alguns parques em concreto.
Conclusão
Devido à elevada contaminação ambiental e à elevada mortalidade (o grupo B tinha chegado aos 18% em pouco mais de um mês desde a sua chegada) – aparentemente sem possibilidade de controlo – a meados de Dezembro decidiu-se vazar completamente as baterias, transferindo todos os leitões do grupo B e C para uma engorda (sítio 3) externa. Uma vez vazias, as baterias foram limpas a fundo utilizando agentes espumantes, lavou-se com água quente à pressão e desinfectou-se. Pese a que o controlo já era bom, reviram-se e reforçaram-se todas as acções de desratização e, como medida de segurança adicional, todas as salas foram submetidas a termonebulização. A exploração manteve-se completamente vazia durante uma semana. A 29 de Dezembro chegou um novo grupo e, nem este nem todos os sucessivos, voltaram a apresentar qualquer sintomatologia compatível com EMCV.
Notas epidemiológicas
A incidência do vírus da encefalomiocardite em porcos domésticos e javalis em vários países Europeus foi descrita em diversos artículos. Numa revisão de 2005, H. Maurice et al (2005), detectaram que a maioria dos focos clínicos aconteceram na Bélgica (320), seguida da Itália (110), Grécia (15) e Chipre (6). Os focos pareciam estar agrupados em "áreas endémicas" com um aumento dos mesmos nos meses de Outono e Inverno. A seroprevalência medida nas exploraçõe afectadas clinicamente variava consideravelmente entre explorações (2-87%), entre várias idades (0-84%) e entre países. Dados procedentes de explorações sem clínica aparente mostraram que a infecção subclínica por EMCV se encontrava tanto dentro (seroprevalência 6-62%) como fora (até 17%) das zonas endémicas dos países clinicamente afectados bem como em países sem clínica da doença, Áustria e Francia (3-5,4%). A seroprevalência nos javalis variava entre 0,6 e 10,8%, e num estudo na Bélgica encontrou-se uma prevalência de infecção pelo vírus de 3,3%.